| Опис |
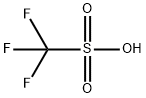
Трифлуорометансулфонска киселина, такође позната као трифлична киселина, ТФМС, ТФСА, ХОТф или ТфОХ, је сулфонска киселина са хемијском формулом ЦФ3СО3Х. Често се сматра једном од најјачих киселина и једна је од бројних такозваних "суперкиселина". користи се у производњи фармацеутских производа, пољопривредних хемикалија и полимера. Анхидровани облик се широко користи у финој хемијској синтези. Неоксидира, има високу термичку стабилност и отпоран је на оксидацију и редукцију, што га чини једним од кориснијих једињења у класи супер киселина. У фармацеутској индустрији, користи се за прављење бројних класа лекова, укључујући нуклеозиде, антибиотике, стероиде, протеине и гликозиде. Трифлиц анхидрид лако реагује са водом и има неповољан профил токсичности. |
| Хемијска својства |
Трифлуорометансулфонска киселина је хигроскопна, безбојна течност на собној температури. Растворљив је у поларним растварачима као што су диметилформамид (ДМФ), диметил сулфоксид (ДМСО), ацетонитрил и диметил сулфон. Додавање трифличне киселине поларним растварачима може бити опасно егзотермно.
Трифлуорометансулфонска киселина се широко користи, посебно као катализатор и прекурсор у органској хемији. Са Ка=8. 0 1014 (пКа ~ -15) мол/кг, ХОТф се квалификује као суперкиселина. Трифлична киселина дугује многа своја корисна својства својој великој термичкој и хемијској стабилности. И киселина и њена коњугирана база ЦФ3СО3-, позната као трифлат, отпорне су на реакције оксидације/редукције, док многе јаке киселине оксидирају, нпр. ХЦлО4 и ХНО3. Трифлат ањон је имун на напад чак и јаких нуклеофила. Због своје отпорности на оксидацију и редукцију, трифлична киселина је веома користан и свестран реагенс. Даље препоручујемо његову употребу, трифлична киселина не сулфонира супстрате, што може бити проблем са сумпорном киселином, флуоросумпорном киселином и хлоросулфонском киселином. Испод је прототип сулфонације, којем ХОТф не пролази: Ц6Х6 + Х2СО4 → Ц6Х5(СО3Х) + Х2О. |
| Припрема |
Жуто-браон течност. Тачка кључања је 167~170 степени. Индекс преламања је 1.331.Релативна густина је 1.708.То је најјача органска киселина, лако растворљива у води.Користите угљен-дисулфид као сировину, са реакцијом јод пентафлуорида да бисте произвели трифлуорометил дисулфид .(ЦФ3С) 2Хг се добија при реакцији са живом; Затим се оксидацијом водоник-оксида добија трифлуорометансулфонска киселина. |
| Користи |
Користи се за органску синтезу, која се широко користи у фармацеутској и хемијској индустрији, као што су нуклеозиди, антибиотици, стероиди, протеини, шећер, синтеза витамина, модификација силиконске гуме.
Изомеризација и алкилација катализатора, припрема 2, 3-дихидро-2-инданона, тетралона, гликозида у уклањању гликопротеина.
|
| Реакције |
Трифлуорометансулфонска киселина делује као катализатор за реакције естерификације и кисели титрант у неводеној киселинско-базној титрацији. Користан је у протонацијама због присуства коњугатне базе, трифлат није нуклеофилан. Служи као средство за дегликозилацију за гликопротеине. Поред тога, он је прекурсор и катализатор у органској хемији. Реагује са ацил халогенидима да би се припремили мешани трифлат анхидриди, који су јаки ацилујући агенси који се користе у Фридел-Крафтсовим реакцијама. Делује као кључни полазни материјал за припрему етра и олефина реакцијом са алкохолима, као и за припрему анхидрида трифлуорометансулфонске киселине реакцијом дехидратације.
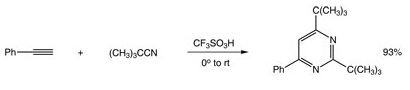
Катализатор који се користи у производњи замене за какао путер од палминог уља. Ово је врло слична реакција ономе што би се урадило ако би неко желео да створи полимере користећи трифличну киселину у синтези. Друге реакције типа Фриедел-Црафтс које користе трифличну киселину укључују крековање алкана и алкилацију алкена који су веома важни за нафтну индустрију. Ови катализатори деривата трифлитне киселине су веома ефикасни у изомеризацији равноланчаних или благо разгранатих угљоводоника који могу повећати октански број одређеног горива на бази нафте. |
| Хемијска својства |
Бистра веома светло жута течност. Дим у ваздуху, лако се апсорбује вода да би се формирао хидрат. Лако је растворљив у води, ослобађа много топлоте и хидролизује да би се добио трифлуорометан (ЦХФ3) и сумпорна киселина. |
| Користи |
Као катализатор у реакцијама ацилације, алкилације и полимеризације типа Фридел-Крафтс; као растварач за ЕСР; као неводени титрант јаке киселине; са трифлуоросирћетном киселином, кв, у чврстој фази пептидне синтезе. Једна од најјачих доступних монопротичних киселина. |
| Користи |
Трифлуорометансулфонска киселина делује као катализатор за реакције естерификације и кисели титрант у неводеној киселинско-базној титрацији. Користан је у протонацијама због присуства коњугатне базе, трифлат није нуклеофилан. Служи као средство за дегликозилацију за гликопротеине. Поред тога, он је прекурсор и катализатор у органској хемији. Реагује са ацил халогенидима да би се припремили мешани трифлат анхидриди, који су јаки ацилујући агенси који се користе у Фридел-Крафтсовим реакцијама. Делује као кључни полазни материјал за припрему етра и олефина реакцијом са алкохолима, као и за припрему анхидрида трифлуорометансулфонске киселине реакцијом дехидратације. |
| Дефиниција |
ЦхЕБИ: Трифлуорометансулфонска киселина је једињење са једним угљеником које је метансулфонска киселина у којој су водоници везани за метил угљеник замењени флуорима. То је једињење са једним угљеником и перфлуороалкансулфонска киселина. То је коњугована киселина трифлата. |
| Општи опис |
Трифлуорометансулфонска киселина је јака органска киселина. Може се припремити реакцијом бис (трифлуорометилтио) живе са Х2O2. О мешању са ХНО3, даје реагенс за нитрирање (нитронијумску со). Овај реагенс је користан за нитрирање ароматичних једињења. Проучавана је његова дисоцијација у различитим органским растварачима. |
| Безбедносни профил |
Корозиван иритант за кожу, очи и слузокоже. Јака киселина. Бурна реакција са ацилхлоридима или ароматичним угљоводоницима развија отровни гас хлороводоника. Када се загреје до распада, емитује токсичне паре Фанд СОк. Види такође ФЛУОРИДИ. |